ANTIBIORÉSISTANCE : Des nanomachines motorisées qui percent les superbactéries
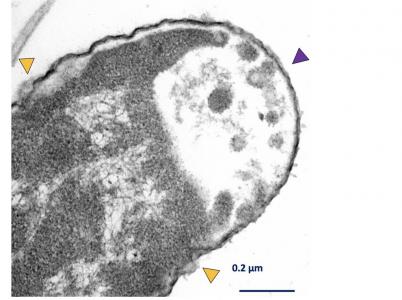
Ces bioingénieurs de la Rice (Texas) ont conçu des moteurs moléculaires qui vont percer ou forer dans les superbactéries et redonnent ainsi une voie et une vie à certains antibactériens. Ces machines moléculaires, présentées dans la revue ACS Nano démontrent ici leur capacité à cibler et à détruire en quelques minutes, des bactéries mortelles qui ont développé une résistance à presque tous les antibiotiques.
Ces superbactéries pourraient tuer 10 millions de personnes par an d'ici 2050 et entrainer ainsi plus de décès que le cancer, expliquent les chercheurs qui ont donc envisagé un tout nouveau système « pour en venir à bout ». En effet, les bactéries savent évoluer de manière à résister aux antibiotiques mais n’ont aucune aucune défense contre des machines « mécaniques » équipées de forets moléculaires qui viennent percer leur enveloppe cellulaire. Les antibiotiques peuvent alors « passer » à travers ces brèches et regagnent en efficacité contre les bactéries.
La machine cible la bactérie et, une fois activée par la lumière, la fore de l’extérieur.
3 millions de rotations par seconde : ces nano-forets sont des molécules qui ressemblent un peu à des pagaies qui se mettent à tourner à 3 millions de rotations par seconde lorsqu'elles sont activées avec la lumière. Les tests montrent effectivement que ces machines moléculaires tuent Klebsiella pneumoniae en quelques minutes. Des images microscopiques des bactéries ciblées permettent de visualiser (voir visuel) où les moteurs ont percé leurs parois cellulaires.
Un foret multicouches ! Le défi est de taille, car les bactéries n'ont pas seulement une double couche lipidique mais aussi une bicouche de protéines avec des sucres qui les relient, donc une paroi cellulaire très robuste. Cela explique aussi pourquoi ces bactéries sont si difficiles à tuer. Mais elles n'ont aucun moyen de se défendre contre une machine « à action mécanique ». Les tests montrent qu’ainsi percée de toutes parts, K. pneumonia redevient sensible au méropénème (carbapénème), un antibactérien auquel la bactérie avait développé une résistance.
La brèche dans l’enveloppe cellulaire est presque imparable : car parfois, lorsqu’une bactérie découvre un médicament, elle ne le laisse pas entrer. Permettre au médicament de passer à travers la paroi cellulaire lui redonne une nouvelle vie. Cela ne résout pas cependant toutes les formes de résistances, car dans certains cas aussi, les bactéries détruisent le médicament en le laissant entrer et en le désactivant.
Des applications immédiates dans le traitement des infections cutanées, des plaies, des cathéters ou des implants : les tests montrent que le ciblage de colonies bactériennes ciblées avec une petite concentration de nanomachines permet d’éliminer jusqu'à 17% des cellules bactériennes, mais ce résultat « grimpe » jusqu’à 65% avec l'ajout de méropénème. Enfin, une optimisation de l’équilibre machines moléculaires et antibiotique permet d’éliminer 94% du pathogène.
« Sur la peau, dans les poumons ou dans le tractus gastro-intestinal, partout où nous pouvons introduire une source de lumière, nous pouvons attaquer ces bactéries », expliquent les chercheurs qui se concentrent actuellement sur le traitement des plaies et des implants infectés. Mais ils envisagent aussi de s’attaquer aux bactéries transmises par la vessie, responsables des infections urinaires.
Et dans le traitement des cancers : Ces nanomachines microscopiques pilotées par la lumière s’attaquent également aux cellules cancéreuses du pancréas : une autre grande avancée, car la lumière visible n'endommage pas autant les cellules environnantes…
Autres actualités sur le même thème
CICATRISATION des PLAIES : Le pansement usagé pour comprendre sa biologie
Actualité publiée il y a 4 années 6 moisLAVAGE des MAINS : A l'eau froide c'est tout aussi antibactérien
Actualité publiée il y a 7 années 10 moisTHÉRAPIE par PRESSION NÉGATIVE: Incisionnelle, elle réduit les complications de plaies post-op
Actualité publiée il y a 8 années 5 moisANTIBIORÉSISTANCE : Sur la piste de l’hydrogène sulfuré
Actualité publiée il y a 3 années 9 mois