COVID-19 : Le candidat médicament qui ferme la porte au virus
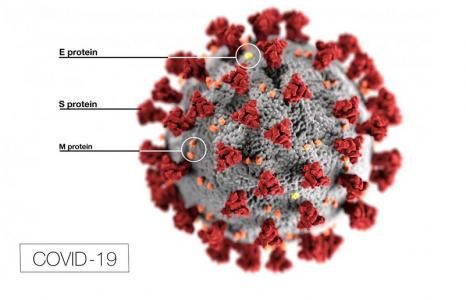
Plusieurs études ont expliqué comment le nouveau coronavirus SARS-CoV-2 se lie aux récepteurs de l'enzyme de conversion de l'angiotensine 2 (ACE2) pour infecter l’hôte apportant ainsi une explication possible des complications pulmonaires graves observées chez certaines personnes diagnostiquées avec COVID-19, atteintes de comorbidités cardiovasculaires préexistantes. Cette équipe de l’Université de la Colombie-Britannique (Canada) propose donc de bloquer la porte cellulaire utilisée par le SRAS-CoV-2 pour infecter ses hôtes. Son candidat, qui cible ainsi ACE2, une protéine de surface cellulaire, récepteur clé de la glycoprotéine de pointe du virus (Spike « S »), promet donc de lui fermer la porte et d’intervenir ainsi dans les tout premiers stades de l’infection.
Le candidat médicament fait ici ses premières preuves d’efficacité in vitro dans des tissus humains infectés, de premiers résultats très positifs qui font dire à l’auteur principal, le Dr Josef Penninger, scientifique à l'UBC, qu’ «il y a de l'espoir pour contrer cette horrible pandémie ». Ainsi, dans ces échantillons de tissus et de cultures, le candidat, nommé à ce stade « APN01 » ou « hrsACE2 » a inhibé la charge virale en la divisant par un facteur 1.000 à 5.000.
Un candidat capable de stopper l'infection précoce
Un résultat prometteur, alors qu’à ce jour, 3 avril, COVID-19 poursuit sa propagation avec plus d’1 million de cas confirmés et plus de 50.000 décès dans le monde.
De plus l’étude, à travers l’observation des effets de la molécule, apporte un nouvel éclairage sur les interactions du virus au niveau cellulaire, et notamment sa capacité d’infection du système cardiovasculaire et des reins.
Au cœur de ce mécanisme, la protéine ACE2, une protéine de surface de la membrane cellulaire, documentée désormais comme un récepteur clé de la glycoprotéine de pointe du SRAS-CoV-2. Dans une précédente étude, l’équipe canadienne avait déjà montré que l'ACE2 est le principal récepteur du SRAS (2003). Au vu des dernières données concernant SARS-CoV-2, l’équipe a cherché à combler l'absence de traitement ciblant spécifiquement ce récepteur critique du SRAS-CoV-2, ACE2 au niveau moléculaire. Le candidat nommé APN01 (enzyme de conversion de l'angiotensine soluble recombinante humaine 2 - hrsACE2) démontre déjà cette capacité in vitro : hrsACE2 inhibe presque totalement la charge virale en la divisant par 1.000 à 5.000.
SARS-CoV-2 cible tout particulièrement le système vasculaire : dans des répliques artificielles (organoïdes) de vaisseaux sanguins et de reins humains, les chercheurs démontrent aussi que le virus peut directement se dupliquer dans ces tissus. Cela fournit des informations importantes sur le développement de la maladie et le fait que les cas graves de COVID-19 présentent une défaillance multi-organes et des signes de lésions cardiovasculaires.
« Avec ces travaux, nous pouvons faire l’hypothèse qu'une forme soluble d'ACE2 qui attrape le virus, pourrait être en effet très prometteuse : une telle thérapie cible en effet spécifiquement la porte que le virus doit emprunter pour nous infecter ».
La molécule sera bientôt testée dans des essais cliniques par la biotech Apeiron Biologics, comme thérapie antivirale prometteuse contre COVID-19.
